先月は、繰り返し充放電ができる“二次電池”の中の“鉛蓄電池”について詳細に調べてみました。引き続き今月も、様々な用途に大量に利用されている二次電池として“ニッケルカドミウム電池”と“ニッケル水素電池”を取り上げます。
(2)ニッケルカドミウム電池
<原理と構造>
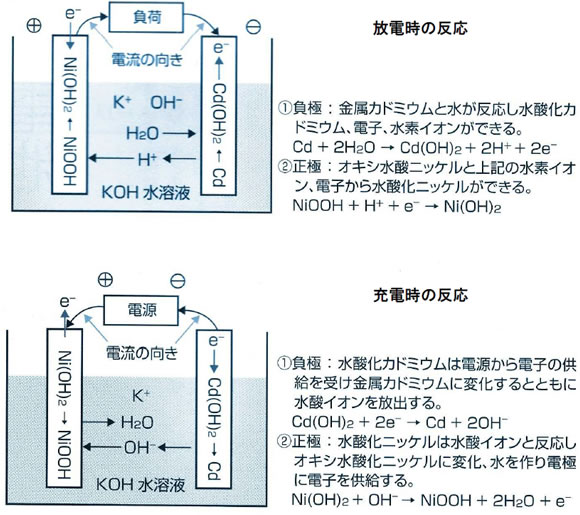
ニッケルカドミウム電池は、正極に水酸化ニッケル(Ni(OH)2)、負極に水酸化カドミウム(Cd(OH)2)、電解液に水酸化カリウム(KOH)を使用する構成の2次電池です。反応の仕組みは次のようになります。
負極では金属カドミウムが水と反応して水酸化カドミウムに変化するとともに電極に電子を供給します。正極では電極から供給された電子を使ってオキシ水酸ニッケルが水酸化ニッケルに変化し、水酸イオンを放出します。放電によって水が消費されるので電解液の濃度が高まり比重が増加します。
充電時の反応は放電時とまったく逆です、負極では電源からの電子の供給を受け、水酸化カドミウム(Cd(OH)2)が金属カドミウム(Cd)に変化し水酸イオン(OH-)を放出します。
正極ではその水酸イオンと電極の水酸化ニッケルが反応し、水酸化ニッケルはオキシ水酸化ニッケル(NiOOH)に変化するとともに水が生成され、電極に電子を供給します。水ができるので、電解液は薄まり比重は低下します。このあたりの事情は鉛蓄電池とは逆になります。
<特徴・活用例>
過充電、過放電に比較的強いという長所がある半面、完全に放電せず継ぎ足し充電をしていると、容量が減少したように見える「メモリー効果」があること、比較的自然放電(漏洩電流)が大きいなどの欠点が指摘されています。公称電圧は1.2Vです。内部抵抗が小さく大電流放電が可能であることから、電動工具などのモーター駆動用によく利用されてきました。また、大型電池は航空機の始動用、車両などの電源やコンピュータ予備電源など広い用途に使用されてきました。
但し、電極に使われているカドミウムは有害物質であるため、廃棄時には流出しないよう管理する必要があり、近年の社会的な環境意識の高まりを受けて需要は減退しています。
電圧の互換性があり、さらに容量が大きく環境負荷の小さなニッケル水素電池の実用化がニッケルカドミウム電池の需要減退を加速することになりました。
(3) ニッケル水素電池
<原理と構造>
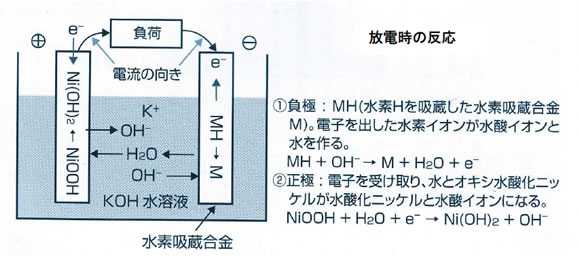
ニッケル水素電池は、正極に水酸化ニッケル(Ni(OH)2)、負極に水素吸蔵合金(M)、これらをセパレータで隔離し、濃アルカリ電解液・水酸化カリウム(KOH)を含浸させて電池缶に密閉化した構造となっています。ニッケルカドミウム電池の負極材料をカドミウムから水素吸蔵合金に変えた構成です。反応の仕組みは次のようになります。
放電時には、負極では電極に蓄えられている水素原子と水酸イオンが、電極の触媒作用によって水に変化するとともに電極に電子を供給します。正極では電極から電子を受け取り、水とオキシ水酸化ニッケルが反応して水酸化ニッケルと水酸イオンが生成されます。充電・放電のプロセスにおいて片側の電極で水が生成され、反対側の電極で水を消費するため電解液の変動はありません。
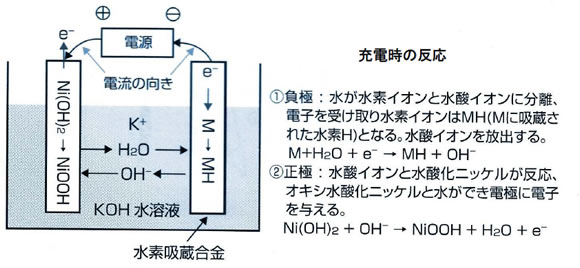
充電時の反応は、放電時とまったく逆になります。充電時の反応は、負極では電極の触媒作用により水を水素イオン(H+)と水酸イオン(OH-)に分解します。水素イオンは電極から与えられた電子を受け取って水素原子となり、そのまま電極である水素吸蔵合金に蓄えられます。正極では水酸イオンと電極の水酸化ニッケルが反応して水酸化ニッケルはオキシ水酸化ニッケル(NiOOH)に変化するとともに、水が生成され電極に電子を供給します。
<負極材料の進歩>
負極の水素吸蔵合金には、Mm(ミッシュメタル=混合希土類金属)-Ni-Co-Mn-Al系合金が広く利用されてきましたが、商品化以来、電池容量は、AAサイズ(単3形)セルで1,100mAh から2,600mAh へと2倍以上に向上し、これ以上の高容量化には、新規高容量合金の導入が必要とされました。また、この合金系では、10質量%程度のCo添加が不可欠であり、これが合金コストの半分を占めることから、コバルトフリー化も求められました。
LaNi系より高容量な合金としては、Ti-Zr-Ni系やV-Ti-Ni系、Mg-Ni系などが検討されましたが、電池特性が十分に改善されず、実用化には至りませんでした。 1997年頃、現在の産業技術総合研究所で、希土類元素とマグネシウム、ニッケルからなる新合金の探索研究の中で、RMg2Ni9(R=希土類)合金が発見されました。これらの合金はAB5ユニットとAB2ユニットとが交互に積層した結晶構造を有しており、従来の1.5倍の水素吸蔵量があることが分かりました。
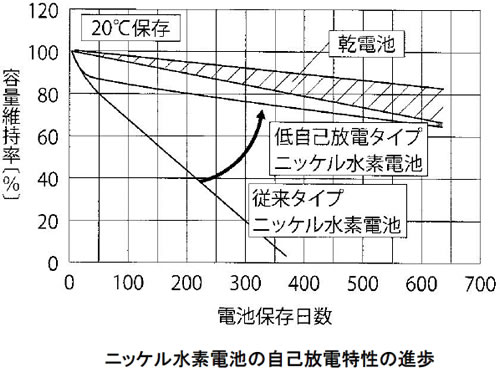
その後、Co添加をしなくても長寿命化できる改善が行われ、従来よりも高容量化したコバルトフリー化新合金(Mm-Mg-Ni-Al系など)が開発されました。また、従来の合金では、CoやMnの溶出が自己放電の要因になっていましたので、新合金では自己放電が顕著に抑制できました(下図参照)。新合金の発見により、Coフリーで、高容量で高出力、長寿命、低自己放電の次世代ニッケル水素電池が実用化されました。自己放電の改善により、充電状態で販売でき、1000回以上使える乾電池代替充電池としての用途が急拡大しています。
<正極材料とセパレータの進歩>
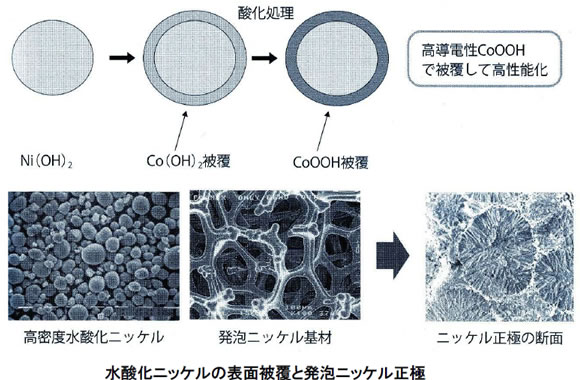
ニッケル正極は、水酸化ニッケル(Ni(OH)2)とオキシ水酸化ニッケル(NiOOH)の反応ですが、それ自体に電子導電性がないため、導電助剤の添加や集電体の工夫が必要となっていました。
1980年代には、携帯機器の普及で、電池高容量化か求められ、発泡ニッケル基材中に高密度水酸化ニッケル粉末を充填した「発泡式電極」が開発されました。さらに、水酸化ニッケルの表面に、電子伝導性のオキシ水酸化コバルトCoOOHを形成して、その集電性を高めています。(下図参照)
セパレータとしては、表面を親水化処理したポリプロピレン系不織布が利用されています(下図参照)。ポリプロピレン系不織布の表面を、熱濃硫酸やフッ素ガスなどで処理して、スルフォン酸基(-SO3)やカルボン酸基(-COOH)、水酸基(-OH)などを付与して親水化することが行われています。これらの表面処理によって、電解液保持性の向上や不純物イオンの吸着除去などが行われ、電池のサイクル寿命や出力特性、自己放電牲吐が大きく改善されています。
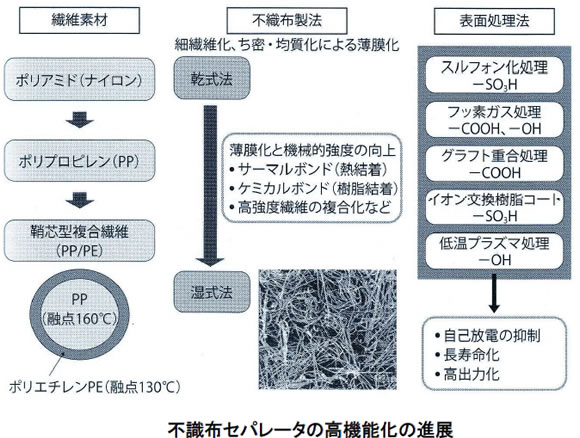
不織布の製法としては、従来は長繊維を乾式でシート化する乾式法が主流でしたが、最近では、薄膜化の要望を受けて、短繊維を水に分散して抄紙する湿式法が主流となっています。セパレータの膜厚としては、100~150μm のものが利用されています。
<特徴・活用例>
公称電圧は1.2V、有害物質であるカドミウムを含んでいないことから、電圧の互換性があるニッケルカドミウム電池からの置き換えが進んでいます。電池容量もはるかに大きく、需要増大を後押ししたようです。ニッケルカドミウム電池と比較した欠点としては、過充電、過放電に弱いとされていますが、充放電制御が一般化しているため問題視されることはありません。自己放電や「メモリー効果」もありますが、ニッケルカドミウム電池よりは軽微です。リチウムイオン電池に比較して大電流放電が可能という特徴を持っています。
用途は多岐にわたり、乾電池代替用、電動工具、ハイブリッド車、産業機器、自然エネルギー利用の電力貯蔵などがあります。
今月は、二次電池の中で、過去のポータブル機器の発展に寄与したニッカド電池、また依然として広範囲な用途で活躍しているニッケル水素電池について、調べてみました。特にニッケル水素電池は電池の中で、水素が動き回って、充放電を繰り返していることが良くお分かりいただけたと思います。次回は、現代の電池の花形であるリチウムイオン電池について、勉強してみたいと思います。
<参考・引用資料>
「図解でナットク!二次電池」 小林哲彦、宮崎義憲、太田 璋 共著(日刊工業新聞社)
「トコトンやさしい2次電池の本」 細田 條 著(日刊工業新聞社)
フリー百科事典ウィキペディア「電池」、「二次電池」
電池工業会ホームページ「電池の知識」
ネオマグ(株)ホームページ「磁石の歴史」

